Атипичные нейролептики (атипичные антипсихотики)
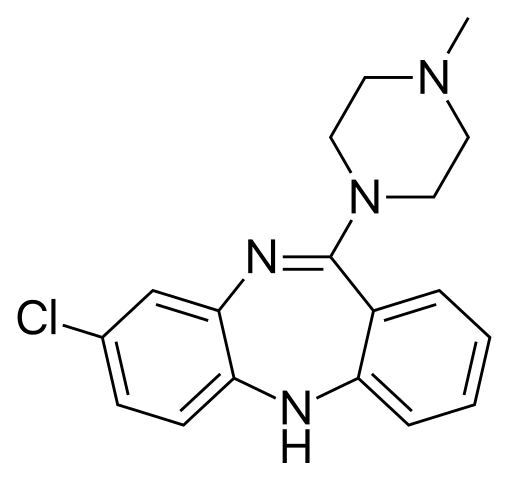
первого из атипичных антипсихотиков
Что такое атипичные нейролептики?
Атипичные нейролептики (атипичные антипсихотики) — новый класс препаратов, самое общее отличие которого от классических (типичных) антипсихотиков заключается в более низкой степени сродства к дофаминовым D2-рецепторам и наличии мультирецепторного профиля связывания (сродства к рецепторам других типов); этим обусловлены их фармакологические свойства, делающие их более «мягкими», в общем случае, более легко переносимыми препаратами.
Общая характеристика
Согласно распространённому представлению, основные различия типичных и атипичных антипсихотиков заключаются в том, что последние не вызывают или редко вызывают экстрапирамидные нарушения. Однако отмечаются и другие характерные для атипичных нейролептиков особенности: значительно меньшая вероятность повышения пролактина (гиперпролактинемии), возникновения так называемого NIDS (нейролептик-индуцированного дефицитарного синдрома) и нейролептической депрессии, положительное влияние на негативную симптоматику и когнитивные нарушения.
Основное действие типичных антипсихотиков связывают преимущественно с их антагонизмом к D2-рецепторам дофамина и снижением нейротрансмиссии в различных дофаминергических системах: антипсихотики угнетают дофаминергическую передачу не только в мезолимбическом нервном пути, но также и в нигростриарном, тубероинфундибулярном и мезокортикальном. Со снижением активности мезолимбических дофаминергических нейронов связывают способность этих препаратов редуцировать психотическую симптоматику, с угнетением дофамина в нигростриарном пути — экстрапирамидные побочные эффекты. Действие типичных нейролептиков на тубероинфундибулярный путь вызывает нейроэндокринные нарушения, в том числе гиперпролактинемию, а угнетение дофамина в мезокортикальном пути и в лобной области коры головного мозга приводит к усилению негативных расстройств (нарастанию апатии, безынициативности), усилению когнитивной дисфункции, возникновению или ускорению прогрессирования дефекта. Особенностью же действия атипичных антипсихотиков является их селективное действие на мезолимбическую дофаминергическую передачу — при минимальном влиянии на нигростриарный путь и тубероинфундибулярный, что снижает вероятность экстрапирамидных, эндокринных и психических побочных эффектов.
Кроме того, для большинства атипичных нейролептиков характерен антагонизм к серотониновым рецепторам второго типа 5-HT2, объясняющий, по мнению некоторых исследователей, терапевтическое влияние (впрочем, недостаточно доказанное) на негативную симптоматику (эмоциональную тупость, безразличие, асоциальность и т. п.) и нарушения мышления. Между серотонином и дофамином существуют реципрокные взаимоотношения, и блокада 5-HT2-рецепторов вызывает высвобождение дофамина в префронтальной коре (психодислептики, например псилоцибин, являются мощнейшими агонистами 5-HT2-рецепторов, то есть оказывают эффект, противоположный атипичным антипсихотикам).
Существуют и другие механизмы, объясняющие характерное для атипичных нейролептиков терапевтическое действие и сравнительно невысокий риск возникновения побочных эффектов. Так, амисульприд (солиан) в низких дозах избирательно блокирует пресинаптические дофаминовые рецепторы, активизируя высвобождение дофамина; в высоких дозах он является эффективным антагонистом постсинаптических дофаминовых рецепторов. Для арипипразола (абилифая) свойствен частичный агонизм к дофаминовым рецепторам: он выступает как функциональный антагонист в мезолимбическом дофаминовом пути, где повышенный уровень дофамина, по мнению исследователей, обуславливает развитие продуктивных симптомов (бреда и галлюцинаций), но является функциональным агонистом в мезокортикальном пути, где снижение активности дофамина, по-видимому, обуславливает развитие негативной симптоматики и когнитивных нарушений.
Отсутствие или малую вероятность возникновения экстрапирамидной симптоматики при приёме атипичных нейролептиков объясняют также низким уровнем связывания этих препаратов с D2-рецепторами в терапевтических дозировках: у пациентов, у которых уровень связывания остаётся ниже 75 %, экстрапирамидные нарушения не возникают. К примеру, уровень связывания D2-рецепторов клозапина (азалептина) в терапевтических дозах находится в пределах 20—67 %. В других случаях низкую вероятность возникновения экстрапирамидных расстройств объясняют высокой степенью сродства к 5-НТ2-рецепторам (при отсутствии чрезмерной блокады D2-рецепторов в терапевтических дозах).
Эти часто отмечаемые различия в действии типичных и атипичных нейролептиков не являются абсолютными. В классе типичных антипсихотиков существуют средства, при приёме которых редко возникают экстрапирамидные нарушения, — например, перициазин (неулептил), тиоридазин (сонапакс); для таких атипичных антипсихотиков, как рисперидон (рисполепт), оланзапин (зипрекса) и зипрасидон (зелдокс), характерен существенный риск экстрапирамидных нарушений, возрастающих при повышении дозы. Рисперидон блокирует D2-рецепторы гипоталамуса и вызывает гиперпролактинемию даже в большей степени, чем классические антипсихотики. Нередко вызывает повышение пролактина и амисульприд; а при приёме зипрасидона, оланзапина повышение пролактина возможно лишь в редких случаях.
В целом класс атипичных нейролептиков характеризуется немалыми различиями, касающимися как механизма действия, так и терапевтической эффективности и побочных действий; можно встретить мнение, что разделение антипсихотиков на типичные и атипичные, вероятно, стоит пересмотреть. Некоторые из нейролептиков (флупентиксол, тиоридазин) одни авторы относят к классическим препаратам, другие — к атипичным. Нет единства мнений и по поводу отнесения к той или иной группе сульпирида (эглонила).
Обладая значительно лучшей переносимостью, чем традиционные антипсихотики, и при этом нередко столь же эффективно купируя психозы, атипичные нейролептики, тем не менее, чаще способны индуцировать метаболические нарушения, приводящие к возникновению ожирения, сахарного диабета, сердечно-сосудистых заболеваний. В некоторых случаях вывод о большей безопасности атипичных нейролептиков по сравнению с типичными был сделан в результате завышения доз препарата, применявшегося в контрольной группе: действие атипичных антипсихотиков сравнивали с действием высоких доз галоперидола, гарантированно дающих тяжёлые побочные эффекты.
Одно рандомизированное контролируемое исследование показало, что метформин может уменьшить набор веса у пациентов, принимающих атипичные антипсихотические препараты, особенно в сочетании с изменением образа жизни (диета и упражнения).
Распространённые атипичные нейролептики
Наиболее распространёнными в мире атипичными антипсихотиками являются азенапин, амисульприд, арипипразол, зипрасидон, илоперидон, кветиапин, клозапин, луразидон, оланзапин, палиперидон, рисперидон и сертиндол.
Сульпирид (Бетамакс, Эглонил) и тиоридазин одни авторы относят к типичным антипсихотикам, другие — к атипичным.
По результатам доклинических испытаний, карипразин обладает прокогнитивной и анти-ангедонической эффективностью, однако достаточный опыт его использования для лечения когнитивных и негативных нарушений отсутствует.
Основные эффекты
Антипсихотическое действие
Атипичные нейролептики не менее эффективны, чем типичные, при лечении продуктивной (галлюцинаторно-бредовой) симптоматики, но, по мнению российских авторов, различаются между собой по профилю психотропного действия — действия на те или иные преобладающие в структуре расстройства синдромы. Эту точку зрения не разделяют западные авторы.
К примеру, российскими авторами высказывается мнение, что при равной общей антипсихотической эффективности для клозапина и оланзапина характерно несколько более выраженное глобальное (инцизивное) антипсихотическое действие, а для рисперидона и амисульприда — избирательное (антибредовое и антигаллюцинаторное).
Существует утверждение, основанное на результатах западных исследований, что атипичные антипсихотики часто бывают эффективны при лечении пациентов, резистентных к терапии типичными антипсихотиками. Однако исследования, подтверждающие это предположение, имели целый ряд методологических недостатков. В достаточной мере доказана лишь высокая эффективность клозапина при резистентных формах шизофрении, но не других атипичных нейролептиков.
Влияние на негативные расстройства
Современные исследования показывают, что атипичные нейролептики не обладают доказанной клинически значимой эффективностью в отношении первичной негативной симптоматики шизофрении (то есть той негативной симптоматики, которая обусловлена непосредственно самим расстройством).
Возможно, что атипичные нейролептики, не влияя на первичную негативную симптоматику, устраняют так называемую вторичную негативную симптоматику благодаря своему антипсихотическому действию (редукции бреда и галлюцинаций у психотических больных), благодаря исчезновению экстрапирамидных нарушений при переводе с типичного нейролептика на атипичный, редукции депрессивной симптоматики, редкости развития затормаживающего действия и редкости развития нейролептической депрессии.
Существует мнение, что у пациентов с первичной негативной симптоматикой всё же эффективно применение амисульприда, но это мнение нуждается в дальнейшем подтверждении.
Влияние на когнитивные функции
Типичные антипсихотики в обычных дозах не обнаруживают благоприятного влияния на когнитивные функции при шизофрении: их склонность к развитию побочных эффектов, таких как экстрапирамидные расстройства, может ещё более усилить когнитивные нарушения. Кроме того, антихолинергические препараты, обычно используемые для лечения экстрапирамидных расстройств, ухудшают познавательные способности, особенно функцию памяти. Антагонизм к α1-адренорецепторам также может нежелательно влиять на когнитивные функции.
Существуют данные в пользу того, что пациенты, принимающие атипичные антипсихотики, показывают лучшие когнитивные результаты, чем пациенты, принимающие классические антипсихотики. С другой стороны, исследования в пользу благоприятного когнитивного эффекта атипичных нейролептиков имеют определённые методологические недостатки, а сравнительные исследования действия на когнитивные функции типичных нейролептиков (в низких дозах) и атипичных нейролептиков не выявили существенных различий, при этом оказавшись методологически более безупречными.
В исследовании года был сделан вывод, что улучшенные показатели могут возникать из-за приспособления пациентов к повторяющимся тестам, представляя собой эффект обучения (англ. practice effect).
Антихолинергические свойства некоторых атипичных нейролептиков (в первую очередь клозапина) и антигистаминные свойства некоторых из этих препаратов могут оказывать неблагоприятное влияние на состояние когнитивных функций. Амисульприд в низких дозах является парциальным агонистом/антагонистом: он повышает сниженную в префронтальной коре дофаминовую активность и, таким образом, может способствовать редукции когнитивных симптомов. Однако в высоких дозах, выступая как антагонист D2-рецепторов, амисульприд приводит к усилению когнитивных нарушений. Арипипразол (абилифай), являясь регулятором дофаминовой активности (парциальным агонистом/антагонистом на всём диапазоне терапевтических доз), воздействует на когнитивные функции, вероятно, наиболее благотворно.
FDA (Food and Drug Administration) включила информацию о когнитивных нарушениях, вызываемых атипичными антипсихотиками, в базы данных по их безопасности.
Влияние на депрессивную симптоматику
Считается, что антидепрессивный эффект некоторых нейролептиков обусловлен блокадой 5-HT1А-рецепторов. По данным опубликованного в году в журнале The Lancet мета-анализа, охватившего 150 двойных слепых исследований, амисульприд, клозапин, оланзапин и арипипразол оказались значительно эффективнее, чем типичные антипсихотики, в способности редуцировать депрессивную симптоматику, в то время как у рисперидона этого превосходства выявить не удалось.
Двухлетнее репрезентативное клиническое исследование показало, что при длительном применении атипичные антипсихотики приводят к постоянному снижению депрессивной симптоматики (измеряемой по шкалам PANSS-D и CDSS). При этом разницы в антидепрессивном воздействии между изучаемыми препаратами (оланзапином, кветиапином, рисперидоном и зипрасидоном) выявлено не было. Согласно данным другого исследования (рандомизированное неслепое испытание продолжительностью 4 мес.), кветиапин превосходил рисперидон по влиянию на выраженность депрессивной симптоматики.
Тем не менее, повышение уровня пролактина при терапии некоторыми атипичными антипсихотиками предположительно может приводить к развитию депрессивных нарушений, враждебности и тревоги. У пациентов с индуцированной типичными нейролептиками гиперпролактинемией нередко наблюдались эмоционально-личностные расстройства, раздражительность, снижение настроения, нарушения сна. По-видимому, те же нарушения могут возникнуть при лечении рисперидоном и такими нетипичными нейролептиками 1-го поколения, как сульпирид и амисульприд. По данным М. Иванова и соавт. (), гиперпролактинемия, индуцируемая нейролептиками, связана с высоким риском развития негативной симптоматики, депрессии, расстройств сна и тревоги.
Согласно данным мета-анализа, при резистентных депрессиях добавление к лечению антидепрессантами группы СИОЗС атипичных антипсихотиков приводит к улучшению, сравнимому с эффектом добавления препаратов лития, однако лечение ими обходится дороже.
Противорецидивное действие
По результатам опубликованного в году мета-анализа, оланзапин, рисперидон и сертиндол демонстрировали в некоторых длительных исследованиях превосходство противорецидивной эффективности над типичными нейролептиками; в случаях амисульприда, арипипразола и клозапина значимого различия по сравнению с типичными антипсихотиками выявлено не было.
Другой мета-анализ, опубликованный в году, тоже обнаружил превосходство некоторых из атипичных антипсихотиков в сравнении с типичными, редуцировавшими частоту рецидивов лишь на 1/3: столь низкий показатель, вероятно, следует объяснить плохим комплайенсом из-за тяжёлых побочных эффектов типичных антипсихотиков. При применении типичных нейролептиков пациенты зачастую нарушают рекомендованный режим амбулаторной терапии, что приводит к быстрому развитию рецидива; при приёме атипичных нейролептиков пациенты в целом лучше соблюдают режим лечения, рецидивы заболевания происходят реже.
Седация и сонливость
Клозапин характеризуется высокой степенью седации; оланзапину и кветиапину присущ умеренный седативный эффект. Рисперидону, амисульприду, зипрасидону и арипипразолу свойственен слабо выраженный седативный эффект, сертиндолу — практически полное отсутствие седации.
В начальном периоде терапии седативный эффект может быть полезным и желаемым результатом у пациентов, страдающих бессонницей, однако долговременная седация способна привести к дистрессу, стать потенциально опасной по причине возможных нарушений суждений, мышления и моторных навыков. Седация может ошибочно трактоваться как негативная симптоматика шизофрении, приводить к ухудшению когнитивного и социального функционирования и к уменьшению возможностей психологической реабилитации пациентов.
Сонливость — очень частый побочный эффект ряда атипичных (клозапин, рисперидон, оланзапин, кветиапин) антипсихотиков. Данный эффект обусловлен, по-видимому, блокадой гистаминовых, дофаминовых и адренорецепторов. Сильнее всего сонливость обычно выражена в начале лечения, при длительном приёме она обычно несколько ослабевает. При наличии у пациента возбуждения этот побочный эффект можно считать скорее терапевтическим, но в дальнейшем выраженная сонливость, особенно дневная, и чрезмерная продолжительность ночного сна становятся помехой для общения, профессиональной деятельности и активного отдыха. Бороться с сонливостью можно снижением дозировки препарата, приёмом суточной дозы на ночь или сменой препарата. Медикаментозное лечение данного побочного эффекта разработано слабо, сравнительно безопасным средством считается кофеин.
Клозапин вызывает сонливость, нередко выраженную и упорную, очень часто. Нередко её вызывает и кветиапин, и в том числе в наиболее низких дозах (100—200 мг/сут.). Оланзапин вызывает сонливость реже, и эффект её дозозависим; дозозависим он и у рисперидона: в обычных дозах (<6 мг/сут.) вероятность сонливости меньше, чем у других атипичных (оланзапин, клозапин, кветиапин) и типичных антипсихотиков.
Экстрапирамидные нарушения
Как правило, мета-анализы показывают меньший риск возникновения экстрапирамидной симптоматики (ЭПС) при применении атипичных антипсихотиков, чем при применении типичных. ЭПС, возникающая на фоне их приёма, является обычно нерезко выраженной и транзиторной (преходящей), она легко корригируется снижением дозы или назначением препаратов-корректоров.
Тем не менее риск ЭПС при назначении атипичных антипсихотиков остаётся значительным. Особенно очевидно это стало при изучении данных побочных эффектов не в рамках клинических исследований, а при сплошной оценке пациентов, получающих нейролептики в реальной клинической практике. Был сделан вывод, что при длительной терапии частота ЭПС на фоне атипичных нейролептиков не отличалась от таковой для низких доз типичных нейролептиков — от 5 до 10 % вне зависимости от препарата. С другой стороны, мета-анализ клинических исследований показал, что общая частота ЭПС при назначении всех антипсихотиков II поколения на 30—50 % ниже, чем при использовании типичных нейролептиков.
Атипичные нейролептики вызывают паркинсонизм и острую дистонию редко. Акатизия является наиболее частым из экстрапирамидных побочных эффектов атипичных антипсихотиков. Она может возникать при применении практически всех антипсихотических средств, включая клозапин; риск её возникновения не связан с выраженностью антидофаминергического эффекта.
Поздняя дискинезия при приёме атипичных нейролептиков развивается редко, однако её нельзя избежать совсем. Систематизированный обзор ( г.) показал, что при лечении атипичными антипсихотиками заболеваемость поздней дискинезией в течение года составляла 0,8 % у взрослых (молодого и среднего возраста), а при лечении типичным антипсихотиком галоперидолом — 5,4 %.
Злокачественный нейролептический синдром также может возникать при приёме практически всех антипсихотиков, в том числе и атипичных, однако наиболее часто вызывают его типичные нейролептики, принадлежащие к группам бутирофенонов, фенотиазинов и тиоксантенов, в особенности галоперидол, флуфеназин (модитен) и хлорпромазин (аминазин).
Рисперидон обладает слабовыраженной дозозависимой способностью вызывать ЭПС, а в дозировках 8—10 мг/сут. — и поздние дискинезии, при этом в дозах свыше 10 мг/сут. риск развития ЭПС на фоне рисперидона сопоставим с риском их при приёме галоперидола. Аналогичный дозозависимый характер свойственен и риску развития ЭПС, в частности паркинсонизма и поздней дискинезии, при приёме амисульприда (особенно в дозах свыше 300 мг/сут.), обладающего сопоставимым неврологическим профилем толерантности с рисперидоном. Сходный риск возникновения ЭПС характерен и для оланзапина (а также, по-видимому, для зипрасидона). Клозапин и кветиапин характеризуются наименьшим риском возникновения этих побочных эффектов.
Повышение уровня пролактина
Все атипичные антипсихотики в той или иной мере могут повышать пролактин, особенно в начале лечения, однако при приёме атипичных нейролептиков гиперпролактинемия в целом развивается реже, чем при приёме типичных. Риск повышения пролактина особенно высок при приёме амисульприда, рисперидона и палиперидона. Рисперидон и амисульприд могут увеличивать уровень пролактина даже в большей мере, чем типичные нейролептики; рисперидон, амисульприд и палиперидон оказывают сильное влияние на уровень пролактина порой даже в низких дозах. Частота возникновения гиперпролактинемии при приёме оланзапина близка к частоте её развития при приёме типичного антипсихотика галоперидола. Кветиапин и арипипразол в большинстве случаев не повышают пролактин.
На основании анализа многочисленных российских и зарубежных исследований был сделан вывод (Горобец Л. Н., ), что по оценке пролактинстимулирующего эффекта (частоты встречаемости нейролептической гиперпролактинемии в сторону убывания) современные антипсихотики можно расположить следующим образом: амисульприд — сульпирид — рисперидон — галоперидол — оланзапин — клозапин — кветиапин — зипрасидон — сертиндол — арипипразол. По другим данным, приём амисульприда вызывает развитие гиперпролактинемии в 80—100 %; рисперидона — в 35—94 %; оланзапина — в 3—52 %; клозапина — в 4—12,5 %; зипразидона — в 2—8,5 % случаев, а терапия кветиапином не сопровождается изменениями уровня пролактина в крови. При терапии рисперидоном, амисульпридом и сульпиридом порой наблюдаются показатели пролактина, в десятки раз превышающие нормативные. При терапии пролонгированными препаратами, такими как Рисполепт Конста (пролонгированный рисперидон), гиперпролактинемия может сохраняться в течение 6 месяцев после отмены препарата.
Гиперпролактинемия снижает секрецию половых гормонов, включая эстрогены и тестостерон, может снизить половое влечение и нарушить половую функцию, у женщин может приводить к нарушению менструального цикла и аменорее, галакторее, отсутствию оргазма, фригидности, вирилизации, себорее волосистой части головы, избыточному слюноотделению, акне, поредению волос. У мужчин признаками гиперпролактинемии являются снижение или отсутствие либидо и потенции, уменьшение вторичных половых признаков, гинекомастия, галакторея, ретроградная или болезненная эякуляция. Как у мужчин, так и у женщин гиперпролактинемия может вызвать бесплодие.
Гиперпролактинемия также приводит к снижению плотности костной ткани, развитию остеопороза, проявлениями которого могут быть частые переломы (переломы шейки бедра, костей дистального отдела предплечья и др.), увеличению массы тела, аутоиммунным нарушениям, водному и электролитному дисбалансу. К возможным последствиям гиперпролактинемии относятся развитие опухоли гипофиза, возникновение сердечно-сосудистых нарушений, сахарного диабета II типа, у женщин повышается риск развития рака молочной железы, фиброзно-кистозной мастопатии, гипоплазии матки.
Психические проявления длительной гиперпролактинемии могут включать в себя депрессию, раздражительность, нарушения сна; могут отмечаться также жалобы неспецифического характера (повышенная утомляемость, слабость, снижение памяти, боли в области сердца без четкой локализации и иррадиации). Могут возникать различные аффективные расстройства, тревожные и тревожно-фобические, соматоформные нарушения, патохарактерологические нарушения (включая нарушения влечений), развиваться сужение интересов, замедление ассоциативных процессов, нарушения концентрации внимания. Возможны и такие проявления, как аутизация, психосоциальная дезадаптация, в некоторых случаях — развитие психоза или ухудшение его течения.
Гиперпролактинемия осложняет течение основного заболевания, усиливает выраженность негативных, когнитивных и аффективных нарушений; она приводит к дополнительной социальной стигматизации пациентов, к развитию аддиктивного поведения, ухудшает качество их жизни и нередко становится причиной отказа пациентов от терапии нейролептиками.
При появлении признаков гиперпролактинемии необходимо снизить дозу нейролептика или перейти на препарат, меньше влияющий на секрецию пролактина. Другой вариант — назначение дофаминомиметика: бромокриптина, амантадина, каберголина или хинаголида.
Для профилактики гиперпролактинемии необходимо регулярно расспрашивать пациентов о симптомах, связанных с повышением уровня пролактина, а при назначении рисперидона или амисульприда (как и при назначении типичных антипсихотиков) регулярно контролировать уровень пролактина в плазме крови. Рекомендуется определять уровень пролактина в крови не реже 1 раза в 2 недели: это позволяет приступить к корректирующим мероприятиям до начала клинических проявлений, которые развиваются в среднем лишь через 10—12 дней после возрастания уровня пролактина.
Некоторые авторы придерживаются мнения, что при бессимптомной (не сопровождающейся клиническими проявлениями) гиперпролактинемии проводить коррекционные мероприятия не обязательно. Однако даже в этом случае таким пациентам требуется тщательное наблюдение, поскольку развития поздних проявлений гиперпролактинемии, в частности остеопороза, полностью исключить нельзя.
У подростков высокий пролактин и обусловленное им подавление выработки половых гормонов может привести к нарушению полового созревания. Как и у взрослых, возможна аменорея и другие нарушения менструального цикла, галакторея, гинекомастия, а также развитие остеопороза. В период полового созревания у подростков при гиперпролактинемии снижается плотность костной ткани, что приводит к нарушениям формирования пика костной массы. Для пациенток с гиперпролактинемией, возникшей в детском или подростковом возрасте, характерен высокий риск развития бесплодия.
Ожирение и метаболические нарушения
Клозапин и оланзапин характеризуются наибольшим риском клинически значимого повышения веса и метаболических нарушений, значительно меньшим риском ожирения характеризуются рисперидон, кветиапин, амисульприд, зотепин, сертиндол, азенапин, илоперидон и палиперидон. Кветиапин, рисперидон и сертиндол чаще, чем арипипразол и амисульприд, вызывают ожирение и метаболические нарушения, а зипразидон — реже, чем арипипразол и амисульприд.
Прибавка в весе при приёме нейролептиков может происходить быстро в первые несколько недель, после чего скорость прибавки веса постепенно снижается до тех пор, пока через несколько месяцев не будет достигнуто плато прироста веса — через 4—9 месяцев для оланзапина и через 42—46 месяцев для клозапина. Считается, что метаболические изменения, происходящие в организме пациента при приёме антипсихотиков, обусловливают быстрое увеличение массы тела, а длительная прибавка (в течение нескольких лет), по всей видимости, вызывается поведенческими факторами: предпочтениями в питании и уровнем физической активности. Существует теория «[скорости] зайца и черепахи», согласно которой одни препараты имеют свойство вызывать быструю прибавку веса с последующим выходом на «плато» — «скорость зайца»; другие же, не обладающие таким потенциалом, при длительном применении тоже приводят к увеличению массы тела в связи с воздействием на образ жизни пациента — «скорость черепахи» (в частности, на уровень физической активности может негативно влиять седативный эффект нейролептиков).
Последствия ожирения, вызванного нейролептиками, по-видимому, ничем не отличаются от последствий ожирения любой другой этиологии: они включают в себя повышенный риск ишемической болезни сердца, артериальной гипертонии, онкологических заболеваний, сахарного диабета, остеоартроза, апноэ во сне, желчекаменной болезни, инфаркта миокарда и инсульта. Средства для борьбы с ожирением разработаны слабо, основную роль играют диета и физические упражнения.
По данным многих исследований, в том числе РКИ, приём клозапина и оланзапина обусловливает повышенный риск сахарного диабета и дислипидемии. Оланзапин в большей мере повышает уровень холестерина, чем кветиапин, кветиапин — в большей мере, чем рисперидон, а рисперидон — в большей мере, чем арипипразол и зипразидон, которые оказывают наименьшее влияние на липидный статус.
Развитие гиперлипидемии на фоне терапии нейролептиками связано, по-видимому, с повышением массы тела, хотя обсуждались и другие возможные механизмы возникновения этого побочного эффекта. Изменения уровня липидов при приёме нейролептиков имеют типично атерогенный характер и заключаются в повышении уровня общего холестерина, триглицеридов, повышении уровня холестерина липопротеинов низкой плотности и снижении уровня холестерина липопротеинов высокой плотности. Гиперлипидемия является основным фактором развития сердечно-сосудистых заболеваний и часто сопровождается диабетом 2-го типа.
Развитие инсулинорезистентности при приёме антипсихотиков может происходить и независимо от изменения массы тела; зачастую возникновение диабета при приёме этих препаратов не обусловлено ожирением.
Некоторые атипичные антипсихотики, в особенности оланзапин и клозапин, могут вызвать диабетический кетоацидоз и гиперосмолярную кому. Возможность диабетического кетоацидоза всегда следует иметь в виду, так как его психические проявления легко спутать с симптомами шизофрении.
При оценивании в исследовании CATIE (Clinical Antipsychotic Trials of Intervention Effectiveness) риска развития ишемической болезни сердца на протяжении 10 лет при приёме антипсихотиков обнаружилось, что повышенный риск развития ИБС связан с приёмом оланзапина и кветиапина, а при приёме рисперидона, зипразидона и типичного нейролептика перфеназина этот риск был ниже.
Редко диагностируемым, однако частым и серьёзным побочным эффектом антипсихотических средств может быть полидипсия — состояние, при котором человек выпивает большое количество (до 20 литров в день) жидкости без чувства жажды и потребности в воде. Переизбыток воды приводит к водной интоксикации: головным болям, расплывчатости зрения, тошноте, сонливости; в тяжёлых случаях к повышению температуры тела, сухости кожи, дрожи, слюнотечению, рвоте, поносу, коме. Полидипсия зачастую не расценивается пациентами и их близкими как болезненное явление, её симптомы могут приписываться сахарному или несахарному диабету.
При диагностике увеличения массы тела особое внимание нужно уделять локализации жировых отложений, особенно их количеству в области живота (абдоминальное ожирение). Для оценки можно использовать такой показатель, как соотношение объёма талии к объему бёдер (WHR): значение WHR более 0,9 для мужчин и более 0,85 для женщин означает наличие избыточного абдоминального жира.
На практике часто также используется понятие «индекс массы тела» (body mass index — BMI): масса тела в килограммах делится на рост в метрах в квадрате. Показателем избыточной массы является ИМТ ≥ 25 кг/м2, при ИМТ ≥ 30 кг/м2 диагностируется ожирение.
Рекомендации по мониторингу риска развития сахарного диабета включают измерение уровня глюкозы натощак или гемоглобина A1c всем пациентам при назначении нового антипсихотика. Уровень глюкозы не должен превышать 126 mg/dl, гемоглобина A1c — 6,1 %. У пациентов с факторами риска (семейный анамнез, избыточный вес) мониторинг уровня глюкозы следует проводить каждые 2—4 мес. Кроме того, психиатр должен регулярно оценивать возможные симптомы сахарного диабета (изменение веса, полиурия, полидипсия) и при необходимости обеспечить пациенту консультацию эндокринолога.
При диагностике диабета желательно учитывать не только уровень гликемии натощак, но и уровень через 2 часа после приёма глюкозы. Это позволяет с большей точностью выявлять как сахарный диабет, так и преддиабетные состояния — нарушенную толерантность к глюкозе. При правильно проводимых мерах профилактики у пациентов с преддиабетным состоянием можно предотвратить развитие в будущем у них диабета.
Измерение уровня липидов пациентам, принимающих антипсихотики, необходимо проводить не реже одного раза в год, а у больных с избыточным весом — один раз в 6 мес. с обязательным консультированием у терапевта.
Необходимые обследования
Действие на сердечно-сосудистую систему
Согласно данным исследований, все антипсихотики существенно различаются по своему влиянию на сердечно-сосудистую систему. При этом их кардиотоксичность может быть связана как с острыми, возникающими на ранних этапах терапии и обычно требующими неотложного вмешательства осложнениями (артериальная гипотония, в том числе ортостатическая, нарушения ритма и проводимости, лекарственный миокардит и т. д.), так и с более отдалёнными последствиями, возникающими после нескольких недель или месяцев терапии, обусловленными влиянием антипсихотических препаратов на те или иные факторы риска сердечно-сосудистых заболеваний: ожирение, гиперлипидемию, анемию и др.
Артериальная гипотония при применении антипсихотиков обычно развивается в начале лечения и при увеличении дозы; в этот период желательно регулярно проводить ортостатическую пробу (измерять артериальное давление в положении стоя и лёжа). При возникновении у пациентов тяжёлой ортостатической гипотонии необходимо предупредить, чтобы они не вставали резко и без посторонней помощи. Особенно тяжёлые последствия ортостатической гипотонии отмечаются у пожилых пациентов и больных ишемической болезнью сердца: в частности, возможно развитие обмороков, сопряжённых с травматизмом (повреждения внутренних органов, переломы, в том числе и шейки бедра, вывихи, гематомы). Гипотония у пациентов, страдающих ишемической болезнью сердца, может способствовать манифестации приступов стенокардии, инфаркта миокарда и даже внезапной смерти.
Медленное повышение дозы, использование низких доз, дробный приём препаратов и использование нейролептиков, не оказывающих антиадренергического действия, помогают уменьшить риск ортостатической гипотонии.
Артериальная гипотония может вызывать рефлекторную тахикардию и в редких случаях приводить к шоку. При заболеваниях сердца может представлять опасность увеличение частоты сердечных сокращений в покое. Тахикардия может также возникать при отсутствии артериальной гипотонии, в этих случаях её можно лечить низкими дозами β-блокаторов (например, атенололом).
Удлинение интервала QT свыше 500 мс при приёме антипсихотиков указывает на риск пируэтной тахикардии, которая может приводить к обмороку, фибрилляции желудочков и смерти. При лечении зипрасидоном необходимо своевременно выявлять факторы риска пируэтной тахикардии: врождённое удлинение интервала QT, брадикардию, гипокалиемию, гипомагниемию, сердечную недостаточность, печёночную и почечную недостаточность, передозировку зипрасидона. Назначение других нейролептиков также следует ограничить у пациентов с синдромом врождённого удлинения интервала QT и пациентов с нарушениями ритма в анамнезе; следует избегать применения нейролептиков на фоне гипокалиемии. Желательно предварять нейролептическую терапию (за исключением наиболее кардиобезопасных препаратов: оланзапин, кветиапин) регистрацией ЭКГ в 12 стандартных отведениях. При лечении антипсихотиками, удлиняющими QT-интервал, желательно проводить повторные исследования концентрации калия и магния, а также регулярное мониторирование ЭКГ (при увеличении QT-интервала более чем на 25 % от нормальных показателей рекомендуется под контролем ЭКГ прекратить терапию или снизить дозу антипсихотика).
В редких случаях на фоне терапии нейролептиками возможно развитие миокардита, имеющего токсический или аллергический характер. В частности, клозапин (которому в наибольшей мере свойствен риск токсико-аллергического воздействия на миокард) может вызывать эозинофилию, сопряжённую с развитием эозинофильной кардиомиопатии.
По данным ретроспективного обсервационного когортного исследования выявлено зависящее от дозы двукратное увеличение риска внезапной сердечной смерти у пациентов, принимавших атипичные нейролептики, по сравнению со сходными случаями среди пациентов, не принимавших антипсихотики.
Антихолинергические побочные эффекты
Антихолинергическое действие нейролептиков проявляется разнообразными симптомами, включая сухость во рту, запор, тахикардию, задержку мочи, расстройства терморегуляции, нарушения аккомодации, обострение закрытоугольной глаукомы. Эти побочные явления часто возникают при терапии клозапином — чаще всего умеренно выраженные, но иногда вызывающие опасные последствия (например, нераспознанная непроходимость кишечника может привести к смерти; в жаркую погоду возможен тепловой удар). В меньшей степени риск развития антихолинергических эффектов характерен для оланзапина. У остальных атипичных антипсихотиков вероятность развития антихолинергических эффектов в процессе лечения невелика, в особенности этот риск незначителен для кветиапина и рисперидона; типичные нейролептики характеризуются существенно более высоким риском данных побочных действий.
Приём клозапина и оланзапина может вследствие антихолинергического действия привести к ухудшению когнитивных функций; антихолинергическое действие нейролептиков может проявляться нарушением внимания, памяти, общим торможением центральной нервной системы. Возможны развитие сонливости, спутанности сознания, а также делирия, галлюцинаций. При применении атипичных антипсихотиков возможен антихолинергический синдром.
Антихолинергические побочные эффекты дозозависимы, их можно устранять снижением дозировки препарата и дробным приёмом антипаркинсонических средств.